A phase II, randomized, double-masked, controlled trial to establish the safety and efficacy of intravitreous injections of e10030 (anti-pdgf pegylated aptamer) given in combination with lucentis® in subjects with neovascular age-related macular degeneration
Los objetivos de este estudio son evaluar la seguridad y la eficacia de la inyección intravítrea de E10030 administrada en combinación con Lucentis® en comparación con un grupo de control tratado únicamente con Lucentis® en pacientes con neovascularización coroidea subfoveal secundaria a una degeneración macular asociada a la edad (DMAE).
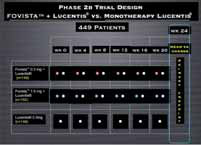


Pacientes aleatorizados a razón de 1:1:1 en los siguientes grupos de dosificación:
- 0,3 mg/ojo de E10030 + Lucentis® 0. 5 mg/ojo
- 1,5 mg/ojo de E10030 + Lucentis® 0. 5 mg/ojo
- E10030 placebo + Lucentis® 0. 5 mg/ojo
Pacientes tratados con E10030 activo o E10030 placebo en combinación con Lucentis® en el día 0 y las semanas 4, 8, 12, 16 y 20. Todos los pacientes tuvieron una visita de seguimiento en la semana 24.
Los pacientes que recibieron la combinación de Fovista (1,5 mg) y Lucentis® ganaron de media 10,6 letras de visión en el optotipo estándar ETDRS a las 24 semanas, a diferencia de las 6,5 letras para los pacientes que recibieron monoterapia de Lucentis® (p = 0,019), lo que representa un beneficio de un 62 % adicional. No se observaron cuestiones de seguridad significativas en ninguno de los dos grupos de tratamiento del ensayo.